Rutoside
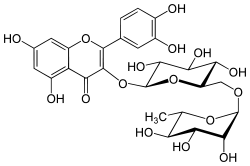
Le rutoside est un diglycoside du quercétol, le 3-O-rutinosylquercétol, assez habituel dans la nature. Il porte aussi les noms de rutine et sophorine.
| Rutoside | |
|---|---|
 |
|
| Général | |
| Nom IUPAC | 2- (3, 4-dihydroxyphenyl) - 4, 5-dihydroxy-3-[3, 4, 5- trihydroxy-6-[ (3, 4, 5- trihydroxy-6-methyl- oxan-2-yl) oxymethyl] oxan-2-yl]oxy-chromen- 7-one |
| Synonymes | Rutine Sophorine 3-O-rutinosylquercétol C. I. Natural Yellow 10 Vitamine P |
| No CAS | |
| No EINECS | |
| Code ATC | |
| PubChem | |
| SMILES |
|
| InChI |
|
| Apparence | cristal jaune |
| Propriétés chimiques | |
| Formule brute | C27H30O16 [Isomères] |
| Masse molaire | 610, 5175 g∙mol-1 C 53, 12 %, H 4, 95 %, O 41, 93 %, |
| Propriétés physiques | |
| T° fusion | 125 °C[1] |
| Solubilité | Faiblement soluble dans l'eau (125 mg·L-1) [1] |
| Précautions | |
|
|
|
|
|
|
| Phrases S : 24/25, | |
| Écotoxicologie | |
| DL50 | 2 000 mg·kg-1, rat, i. p. 950 mg·kg-1, souris, i. v. [1] |
| Composés apparentés | |
| Autres composés | Quercétol, Kæmpférol |
|
|
|
Le rutoside est un diglycoside du quercétol, le 3-O-rutinosylquercétol[2], assez habituel dans la nature. Il porte aussi les noms de rutine et sophorine. C'est un flavonoïde naturel de type flavonol qui possède des propriétés pharmacologiques intéressantes. Il est hydrolysé en quercétol dans le tractus gastro-intestinal.
Le nom de rutine vient de sa présence dans la rue officinale (Ruta graveolens), un arbrisseau particulièrement aromatique de la garrigue méditerranéenne.
Plantes riches en rutoside[3]
- Sophora japonica : le sophora est un grand arbre de la famille des Fabacées, venant de Chine, cultivé en Europe à des fins ornementales. L'industrie pharmaceutique l'utilise pour ses boutons floraux[4] qui contiennent juste avant leur épanouissement, de 15 à 20% de rutoside. Avant l'arrivée des colorants synthétiques, il était aussi utilisé en Asie Orientale pour teindre la soie.
- le sarrasin (Fagopyrum esculentum) est une pseudocéréale annuelle de la famille des Polygonacées, cultivée pour ses graines alimentaires. Ses feuilles contiennent de 2 à 3% de rutoside et les variétés perfectionnées jusqu'à 5-8% mais la présence de substances photosensiblisantes (fagopyrines) compliquent l'extraction.
- Eucalyptus macrorrhyncha a les feuilles suffisamment riche en rutoside pour en permettre l'extraction[5].
- la pensée sauvage (Viola tricolor), avec 23% de rutoside est la plante la mieux pourvue[6]
- le murier blanc (Morus alba) dont les feuilles contiennent 6% de rutoside
- le persil (Petroselimum crispum) est aussi riche (3% dans ses feuilles)
- la rhubarbe (Rheum rhabarbarum) contient la plupart de phénols dont le rutoside (0, 6% dans les feuilles)
- la myrtille (Vaccinum myrtillus) a des baies dont le contenu total en flavonols est compris entre 540 et 1300 mg d'équivalent de rutoside par kilo de matière sèche
- les asperges : c'est un légume ayant une des plus grande activité antioxydante parmi 43 légumes et le rutoside est leur flavonoïde principal (450mg/kg du poids frais des asperges blanches) [7]
- les oignons sont une source majeure de flavonols et surtout de quercétol et de ses glycosides comme le rutoside
- le ginkgo (Ginkgo biloba), riche en quercétol et rutoside
- le coing (Cydonia oblonga), le tabac, le forsythia, etc.
Absorption et métabolisme
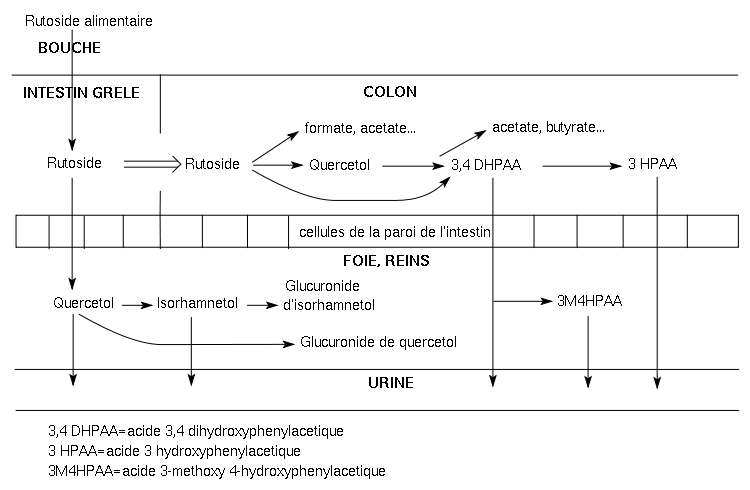
Seule une petite fraction (17%) du rutoside est absorbée dans l'intestin grêle, le reste (83%) passe dans le colon où il est métabolisé. Le rutoside y est en premier lieu déglycolisé en quercétol. Les bactéries de la microflore du colon clivent aussi le rutoside et le quercétol en acides phénylacétiques (acide 3, 4-dihydroxyphénylacétique 3, 4DHPAA, acide 3-hydroxyphénylacétique 3HPAA), ainsi qu'en formate, acétate, butyrate, etc. et divers produits intermédiaires tel le phloroglucinol. La bactérie fécale responsable du clivage du rutoside a été identifiée comme étant Eubacterium ramulus[8].
Une fois absorbés, ces métabolites sont conduits par le sang dans le foie et les reins où ils subissent une méthylation et une glucuronisation.
|
|
Les métabolites en acides phénylacétiques ont une moindre activité anti-oxydante que les composés dont ils sont issus. De plus, seul le 3, 4DHPPAA montre une activité antiproliférative sur les cellules du cancer du colon et de la prostate. [9], [10] [11].
Activités biologiques
De nombreuses études ont montré que le rutoside était capable de piéger les radicaux libres [12], d'être pourvu d'une puissante activité anti-oxydante [7], d'avoir des effets anti-inflammatoires [13], d'avoir des propriétés anticancéreuses [14] [15] et de diminuer la cytotoxicité de la lipoprotéine LDL (le mauvais cholestérol) oxydé [16]. L'activité anti-oxydante du rutoside est du même ordre de grandeur que celle du quercétol, elle est moindre que celle du myricétol et supérieure à celle du kæmpférol. [17] :
Myricétol > Quercétol, Rutoside > Kæmpférol
Sawa et als. (1999) [18] ont montré que la puissante activité de piégeur de radicaux libres in vitro du rutoside pourrait jouer un rôle dans la protection contre quelques cancers.
Une étude de Koda et als. (2008) [19]a établi que le rutoside avait un effet protecteur contre les déficits de mémoire spatiale induite chez le rat par la perte de cellules pyramidales de la région CA3 de l'hippocampe.
Utilisations diététiques et thérapeutiques
De nombreuses études épidémiologiques ont montré que la consommation régulière de fruits et légumes riches en flavonoïdes était clairement liée à une diminution des risques de maladies cardiovasculaires, neurologiques et cancéreuses [20]. L'identification des principes actifs permettra de passer de la diététique aux utilisations thérapeutiques. Mais pour le moment, la majorité des études étant des tests biochimiques in vitro ou des études de pharmacologie animale, les essais chez l'homme trop rares ne permettent pas d'établir la réelle efficacité clinique des composés flavonoïques.
Une étude de Bamigboye et Hofmeyr[21] (2006) a montré que la prise de comprimés de rutoside par des femmes enceintes pouvait perfectionner les symptômes associés aux œdèmes des membres inférieurs ainsi qu'aux varices. Une réduction de l'œdème de la patte a aussi été obtenue chez la souris souffrant d'arthrite septique[22]. L'efficacité du composé pourrait provenir d'une inhibition de la production de NO par les macrophages et de la prolifération des lymphocytes T.
Une étude pilote[23] a montré les effets bénéfiques de la prise orale de rutoside et d'acide ascorbique sur le purpura progressif pigmenté.
Jean Bruneton[4] résume les utilisations thérapeutiques du rutoside, seul ou associé (esculoside, citroflavonoïdes, acide ascorbique, etc. ) en quatre types d'emplois :
- «dans les manifestations fonctionnelles de l'insuffisance veinolymphatique,
- dans le traitement symptomatique des troubles fonctionnels de la fragilité capillaire,
- dans le traitement des signes fonctionnels liés à la crise hémorroïdaire,
- en cas de baisse d'acuité et de troubles du champ visuel présumé d'origine vasculaire.
Rutoside et dérivés sont quelquefois associés à des alcaloïdes (ex. : vincamicine) dans des spécialités proposées pour perfectionner certains symptômes au cours du déficit intellectuel pathologique du sujet âgé».
Le rutoside est utilisé dans les industries chimique, cosmétique et d'aliments pour animaux comme pigment naturel et conservateur alimentaire.
Notes et références
- (en) ChemIDplus, «Rutin - RN : 153-18-4» sur chem. sis. nlm. nih. gov, U. S. National Library of Medicine. Consulté le 23/07/2008.
- ↑ Le rutinose est le 6-O-L-rhamnosyl-D-glucose
- ↑ (en) Fereidoon Shahidi, Marian Naczk, Phenolics in Food and Nutraceuticals, CRC Press, 2004 (ISBN 1-58716-138-9)
- Jean Bruneton, Pharmacognosie - Phytochimie, Plantes médicinales, Editions Tec & Doc, Editions médicales internationnales, 1999, 1120 p. (ISBN 2-7430-0315-4)
- ↑ [1]
- ↑ Dr. Duke's Phytochemical and Ethnobotanical Databases
- (en) Jianxiong Yang, Juan Guo, Jiangfeng Yuan, «In vitro antioxidant properties of rutin», dans LWT - Food Science and Technology, vol. 41, 2008, p. 1060-1066 [[doi :10.1016/j. lwt. 2007.06.010 texte intégral]]
- ↑ (en) Schneider, H., Schwiertz, A., Collins, M. D., Blaut, M., «Anærobic transformation of quercetin-3-glucoside by bacteria from the human intestinal tract», dans Archives of Microbiology, vol. 171, 1999, p. 81-91
- ↑ (en) Winter J., Lilian H. M., Dowel V. R., Bokkenheuser V. D., «C-ring cleavage of flavonoids by human intestinal bacteria», dans Applied and Environmental Microbiology, vol. 55, 1989, p. 1203-1208
- ↑ (en) M. R. Olthof, P. C. Hollman, M. N. C. P. Buijsman, J. M. M. van Amelsvoort and M. B. Katan, «Chlorogenic acid, quercetin-3-rutinoside and black tea phenols are extensively metabolized in humans», dans The Journal of Nutrition, vol. 133, 2003, p. 1806-1814
- ↑ (en) Jaganath IB, Mullen W, Edwards CA, Crozier A., «The relative contribution of the small and large intestine to the absorption and metabolism of rutin in man. », dans Free Radical Research, vol. 40, no 10, 2006, p. 1035-1046
- ↑ (en) Kandaswami C, Middleton E., «Free radical scavenging and antioxidant activity of plant flavonoids. », dans Adv Exp Med Biol, no 336, 1994, p. 351-76
- ↑ (en) Guardia T, Rotelli Æ, Juarez AO, Pelzer LE, «Anti-inflammatory properties of plant flavonoids. Effects of rutin, quercetin and hesperidin on adjuvant arthritis in rat. », dans Farmaco, vol. 56, 2001, p. 683-7
- ↑ Deschner EE, Ruperto JF, WongGY, et al, «The effect of dietary quercetin and rutin on AOM-induced acute colonic epithelial abnormalities in mice fed a high-fat diet», dans Nutr Cancer, vol. 20, 1993, p. 199-204
- ↑ Jing-Pin Lina, Jai-Sing Yangb, Chi-Cheng Luc, Jo-Hua Chiangc, Chang-LinWud, Jen-Jyh Line, Hui-Lu Linf, Mei-Due Yangg, Kuo-Ching Liuh, Tsan-Hung Chiui, Jing-Gung Chungd, «Rutin inhibits the proliferation of murine leukemia WEHI-3 cells in vivo and promotes immune response in vivo», dans Leukemia Research, 2008 [[doi :10.1016/j. leukres. 2008.09.032 texte intégral]]
- ↑ (en) Milde, J., Elstner, E. F., & GraXmann, J., «Synergistic inhibition of low-density lipoprotein oxidation by rutin, g-terpinene, and ascorbic acid», dans Phytomedicine, vol. 11, 2004, p. 105-113
- ↑ (en) Jessica Tabart, Claire Kevers, Joël Pincemail, Jean-Olivier Defraigne et Jacques Dommes, «Comparative antioxidant capacities of phenolic compounds meausured by various tests», dans Food Chemistry, vol. 113, 2009, p. 1226-1233
- ↑ (en) Sawa, T., Nakao, M., Akaike, T., Ono, K, and Mæda, H., «Alkylperoxyl radical scavenging activity of various flavonoids and other phenolics compounds : implication for the antitumor-promoter effects of vegetables», dans Journal of agricultural and food chemistry, vol. 47, 1999, p. 397-402
- ↑ (en) Tomoko Koda, Yoshiki Kuroda, Hideki Imai, «Protective effect of rutin against spatial memory impairment induced by trimethyltin in rats», dans Nutrition Research, vol. 28, 2008, p. 629-634
- ↑ (en) Willet, W. C., Eat, drink, and be healthy – The Harvard Medical School guide to healthy eating. , Simon and Schuster., New York, 2001
- ↑ (en) Bamigboye A. A., Hofmeyr G. J., «Interventions for leg edema and varicosities in pregnancy. What evidence?», dans European journal of obstetrics, gynecology, and reproductive biology, vol. 129, no 1, 2006, p. 3-8
- ↑ (en) Han Y., «Rutin has therapeutic effect on septic arthritis caused by Candida albicans», dans Mondial Immunopharmacology , 2008
- ↑ (en) Reinhold U, Seiter S, Ugurel S, Tilgen W., «Treatment of progressive pigmented purpura with oral bioflavonoids and ascorbic acid : an open pilot study in 3 patients. », dans Journal of the American Academy of Dermatology, vol. 41, 1999
Voir aussi
Liens externes
Recherche sur Google Images : |
|
"Voie métabolique du rutoside," L'image ci-contre est extraite du site fr.wikipedia.org Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (750 x 490 - 15 ko - png)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité