Ose
Les ose s sont les monomères des glucides. Ils ne sont pas hydrolysables. Tout comme les diholosides, ils possèdent un pouvoir sucrant, et sont solubles dans l'eau.
Recherche sur Google Images :

Source image : decitre.fr Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Définitions :
- Ou monosaccharide, glucide le plus simple, non hydrolysable. (source : stl_bjb.ac-dijon)
Les oses (ou monosaccharides) sont les monomères des glucides. Ils ne sont pas hydrolysables. Tout comme les
- Les trioses oses à 3 carbones, C3H6O3 (glycéraldéhyde, dihydroxyacétone)
- Les tétroses oses à 4 carbones, C4H8O4 (érythrose, thréose, érythrulose)
- Les pentoses oses à 5 carbones, C5H10O5 (désoxyribose, ribose, arabinose, xylose, lyxose, ribulose, xylulose)
- Les hexoses oses à 6 carbones, C6H12O6 (allose, altrose, glucose, mannose, gulose, idose, galactose, talose, psicose, fructose, sorbose, tagatose)
- Les heptoses : oses à 7 carbones, C7H14O7 sédoheptulose, mannoheptulose.
Propriétés physiques
Quelques uns ont une saveur agréable sucrée. Cependant il est faux de généraliser cette propriété : l'amidon par exemple, n'a aucun pouvoir sucrant. À l'inverse, d'autres composés n'étant pas des oses, tels la glycine ou l'acide aspartique (duquel dérive l'aspartame, bien connu des personnes surveillant leur ligne) par exemple, possèdent une saveur sucrée. Les oses sont d'autre part de couleur blanchâtre et sont aisément cristallisables.
Structure
Formule brute
Cn (H2O) n où n est un nombre entier représentant le nombre de carbones (de 3 à 7 pour les oses naturels) pour de nombreux oses, cependant il ne faut pas généraliser cette propriété. A titre d'exemple, l'acide acétique, qui n'est en aucun cas un ose possède la formule brute CH3COOH soit C2 (H2O) 2. D'autre part, des dérivés d'ose, comme la glucosamine (qui possède d'autres atomes que le carbone, l'hydrogène et l'oxygène ; en l'occurrence, l'azote) ne présentent pas la propriété énoncée ci dessus valable pour de nombreux oses.
Structure acyclique
Un ose à n carbones se compose d'une chaîne carbonée non ramifiée, de 3 à 7 carbones, ne comportant que des liaisons simples. L'ensemble des carbones portent une fonction alcool (OH) sauf un qui porte une fonction carbonyle.
Cela détermine par conséquent deux catégories d'oses :
- si la fonction carbonyle est une fonction aldéhyde, elle se trouve sur le premier carbone et c'est un aldose (par exemple le glucose).
- si la fonction carbonyle est une fonction cétone, elle se trouve sur le second carbone, et c'est un cétose (par exemple le fructose).
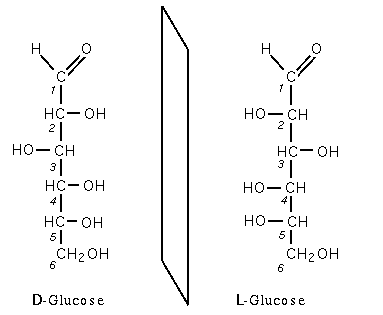
Tous les oses possèdent un pouvoir rotatoire du fait de la présence d'au moins un carbone asymétrique : les oses sont dits chiraux. De fait, s'il y a x atomes de carbone asymétriques, il existe 2x paires d'énantiomères, diastéréoisomères entre elles. Chaque paire a un nom différent et les descripteurs D et L sont habituellement utilisés pour différencier chaque énantiomère.
Deux énantiomères (antipodes optiques) ont les mêmes propriétés à l'exception d'une seule : leur pouvoir rotatoire opposé. La figure 1 représente les deux énantiomères du glucose, la forme D-glucose est la forme naturelle.
- Dans la forme D, le groupement alcool (-OH) porté par le carbone n − 1 est à droite (en représentation de Fischer) ;
- Dans la forme L, le groupement alcool (-OH) porté par le carbone n − 1 est à gauche (en représentation de Fischer).
Structure cyclique
La projection de Haworth est fréquemment utilisée pour représenter la forme cyclique des oses.
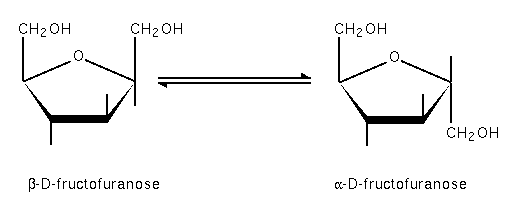
Il y a hémiacétalisation entre la fonction carbonyle et un OH, par conséquent qu'ils sont distants d'au moins 3 carbones. (Ex : entre le carbone 1 et 5 du glucose ou entre le carbone 2 et 5 du fructose, ou encore entre le carbone 1 et 4 du ribose). Le OH né de la cyclisation est nommé OH anomérique ou anomère. Il donne lieu à un nouveau carbone asymétrique (le carbone porteur de la fonction carbonyle : n°1 dans le cas d'un aldose ou n°2 dans le cas d'un cétose) et selon qu'il est positionné sous ou sur le plan du cycle il donne naissance à deux isomères alpha (α) ou beta (β) (alpha signifiant en dessous ; et beta au dessus).
Une fois la chaîne carbonée repliée, la proximité de la double liaison de la fonction aldéhyde (ou cétone s'il s'était agit d'un cétose) permet, du fait de sa fragilité, la rupture de la liaison P et de la liaison OH de la fonction alcool (ici du C n°5), donnant la possibilité l'établissement d'une nouvelle liaison C n°1 et O de l'ancienne fonction alcool du C n°5, fermant ainsi un cycle.
Cycle sous forme furanique
Les oses se cyclisant le plus souvent sous forme furanique (furane) sont :
- Le ribose donnant du ribofuranose ;
- Le 2-désoxyribose donnant du 2-désoxyribofuranose ;
- Le fructose donnant du fructofuranose.
Cycle sous forme pyranique
Les oses se cyclisant le plus souvent sous forme pyranique (pyrane) sont :
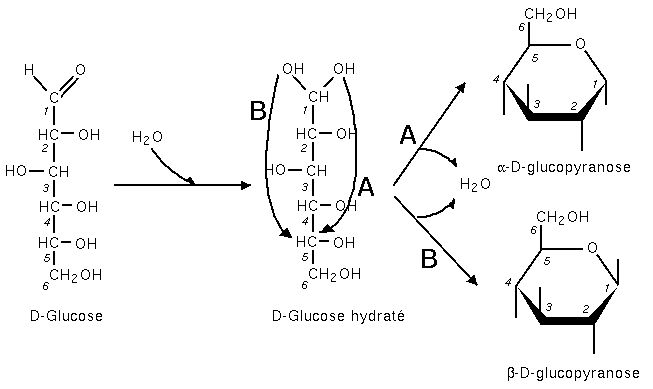
En série D, les formes béta ont toujours leur fonction alcool vers le haut sous la représentation de haworth.
Nomenclature
Ils peuvent se présenter sous forme cristalline. Les oses sont de deux types :
- Si la fonction carbonyle de l'ose est un aldéhyde c'est un aldose.
- Si cette fonction est une cétone, c'est un cétose (ou cétulose).
Les dérivés d'oses
Les polyalcools
Les polyalcools (ou polyols), sont obtenus par réduction de la fonction aldéhyde en alcool, c'est le cas par exemple du glycérol.
Les osamines
Dans les
Les désoxyoses ou désoses
Ils sont créés par substitution d'hydrogène à la place du groupement hydroxyle, on peut noter l'exemple du désoxyribose.
Les acides aldoniques
Ils sont constitués par une oxydation dite "douce" (Exemples d'oxydants doux : Le réactif de Tollens ou la liqueur de Fehling) des aldoses et sont caractérisés par l'oxydation de la fonction aldéhyde en fonction carboxyle. Exemple : Acide Gluconique
Voir aussi
Liens externes
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité