Dihydroxyacétone
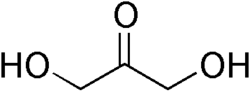
Le dihydroxyacétone, ou DHA, est un ose de formule brute est C 3 H 6 O 3.
| Dihydroxyacetone | |
|---|---|
 |
|
| Général | |
| Nom IUPAC | 1, 3-Dihydroxy-2-propanone |
| Synonymes | Dihydroxyacetone; DHA |
| No CAS | |
| No EINECS | |
| PubChem | |
| FEMA | |
| SMILES |
|
| InChI |
|
| Apparence | Poudre blanche cristalline |
| Propriétés chimiques | |
| Formule brute | C3H6O3 [Isomères] |
| Masse molaire | 90, 0779 g∙mol-1 C 40 %, H 6, 71 %, O 53, 29 %, |
| Propriétés physiques | |
| T° fusion | 75 à 80 °C |
| T° ébullition | 586 °C |
| Solubilité | Eau 1 :1 Ethanol 1 :15 |
| Écotoxicologie | |
| DL50 | 16 g/kg (voie orale) |
|
|
|
Le dihydroxyacétone, ou DHA, est un
Le dihydroxyacétone se compose de trois atomes de carbone, ce qui en fait un triose. C'est un cétose car son groupement carbonyle est localisé en milieu de chaîne carbonée. A l'inverse de son isomère aldose, le glycéraldéhyde, ce n'est pas une molécule chirale, dans la mesure où elle ne possède aucun carbone asymétrique.
Une des caractéristiques du dihydroxyacétone est que ses groupes fonctionnels possèdent des éléments de symétrie. La molécule elle-même présente une symétrie axiale, c'est-à-dire qu'elle est superposable à son image dans un miroir (l'oxygène porté par le second carbone est positionné à droite à titre indicatif), caractéristique qui en fait une exception parmi les
Schéma de la molécule :
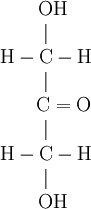
Elle est produite naturellement par bioconversion bactérienne de glycérol.
Utilisations esthétiques
Obtenue le plus souvent du maïs ou de la canne à sucre, la DHA est souvent utilisée en cosmétique, surtout elle forme la molécule pour l'élaboration des autobronzants actuels. La DHA agit par réaction de Maillard sur les kératines de la couche cornée de la peau, créant ainsi un hâle d'aspect plus naturel que les classiques autobronzants donnant une couleur dans les tons orange. Le renouvellement habituel de la couche cornée (composée essentiellement de cellules mortes) explique la disparition progressive de la coloration.
Cette méthode de bronzage artificiel ne fait nullement intervenir les mélanocytes et il n'y a pas production de mélanine. Le brunissement par application de DHA n'a par conséquent pour ainsi dire pas d'effet protecteur vis-à-vis des radiations ultraviolettes comme celui assuré par la mélanine. Il y a absorption occasionnellementdes UVA[1], faiblement énergétiques, mais non des UVB, véhiculant une énergie plus importante, qui représente un plus grand danger de l'exposition au soleil.
Du fait de sa non-pénétration au delà de la couche cornée, aucun effet secondaire gênant n'est aujourd'hui connu à l'application de DHA sur la peau. Une coloration accrue des comédons («points noirs») peut être observée.
Dihydroxyacétone phosphate
La dihydroxyacétone phosphate ou phosphodihydroxyacétone (PDHA), est un des intermédiaires de la glycolyse.
Schéma de la molécule, le groupement phosphate étant en rouge :
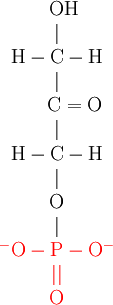
La PDHA est produite par clivage aldolique du fructose-1, 6-bisphosphate avec comme coproduit le glycéraldéhyde-3-phosphate. C'est une réaction réversible dont l'enzyme est l'aldolase.
Comme seul le glycéraldéhyde-3-phosphate est substrat pour la suite de la glycolyse, la PDHA est entièrement transformé en glycéraldéhyde-3-phosphate par isomérisation.
Schéma de la réaction :
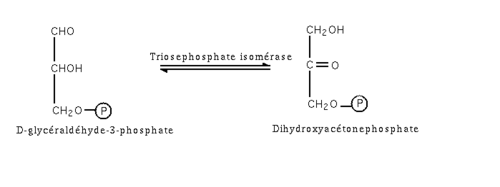
Cette réaction est catalysée par la triose phosphate isomérase. Cet enzyme est reconnu comme ayant atteint la perfection cinétique, c'est-à-dire que le quotient de sa constante catalytique par sa constante de Michælis tend vers 1. Cela se traduit par le fait que seule la concentration en réactant disponible limite son activité.
Références
Liens externes
Recherche sur Google Images : |
|
"File:Dihydroxyacetone" L'image ci-contre est extraite du site commons.wikimedia.org Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (800 x 349 - 23 ko - )Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 05/11/2009.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité